前回、エピジェネティック・リプログラミングが「若返り」を創薬として成立させるための条件と課題を検討しました。細胞のエピゲノムを巻き戻すという発想は、生体システムの「状態」そのものを変えようとする試みです。今回は、それとは異なるもうひとつのアプローチを取り上げます。老化した細胞を除去する「セノリティクス(Senolytics)」です。
Unity Biotechnology 失敗の教訓
細胞老化とは、細胞が不可逆的に分裂を停止しながらも、アポトーシス(細胞死)には至らず、組織内に留まり続ける状態を指します。これらの細胞は老化関連分泌形質と呼ばれる炎症性サイトカインやケモカインを持続的に放出し、周囲の健全な細胞や組織に慢性炎症を引き起こします。
細胞老化は本来は防御機構です。DNA損傷を受けた細胞ががん化する前に分裂を停止し、免疫系によって除去されるのを待ちます。傷害治療の過程でも、一時的な細胞老化が組織修復に寄与します。しかし、加齢に伴って免疫機能が低下すると、老化細胞は除去されず蓄積し、慢性炎症を駆動します。近年、これが動脈硬化、線維化、神経変性、代謝異常といった老化関連疾患の共通基盤として浮上してきました。
セノリティクスとは、蓄積した老化細胞を選択的に除去する薬剤のことです。老化細胞がアポトーシスに抵抗するために依存する生存経路を一時的に阻害することで、老化細胞のみを死滅に導きます。通常細胞はそうした経路に依存していないため影響を受けにくい、というのが理論的前提です。
セノリティクス領域について議論するうえで、米Unity Biotechnologyの事業停止の話題は避けて通れません。Jeff Bezos氏やPeter Thiel氏らの支援を受けて2018年にIPO(新規株式公開)を果たした同社は、「最初の走者」としてこの領域全体の期待を背負っていました。
しかし、変形性関節症を対象とした「UBX0101」の臨床第2相(P2)試験に失敗し、網膜疾患を対象とした「UBX1325」のP2b試験でも主要評価項目を達成できませんでした。結局、同社は2025年5月に全従業員を解雇して事業を停止。8月には上場廃止となり、9月に清算・解散が承認されました。
Unityの失敗から引き出すべき教訓はいくつかあります。
1つ目は局所投与の限界です。同社は一貫してセノリティクスを特定組織に局所投与する戦略をとりましたが、老化細胞の蓄積が全身性の現象である以上、局所介入だけでは十分な効果を示せなかった可能性があります。
2つ目はバイオマーカーの欠如です。老化細胞負荷を定量的に測定し、介入の効果を評価する確立されたバイオマーカーがなければ、臨床試験の設計が脆弱になります。
3つ目は、資金環境の影響です。バイオテック全体の資金調達環境が悪化するなか、老化という未確立の適応症を追求する小規模企業は、投資家を説得するのが困難でした。
かといって、Unityの失敗がセノリティクスという概念そのものの失敗を意味するわけではありません。むしろ、その教訓を踏まえた次世代のアプローチが、すでに動き始めています。
ダサチニブ+ケルセチン
セノリティクス研究の原点とも言えるのが、ダサチニブ(チロシンキナーゼ阻害薬)とケルセチン(フラボノイド)の併用療法です。米Mayo ClinicのJames Kirkland氏らが2015年に報告したこの組み合わせは、既存薬のリポジショニングという実利的なアプローチにより、セノリティクスの概念実証を前進させてきました。
2025年には、ダサチニブ+ケルセチンの複数の臨床試験結果が報告されました。特筆すべきは、軽度認知障害を対象としたパイロット試験の結果です。12週間の間歇的投与後、血漿TNF-αの低下が認知機能の改善と有意に相関しました。アルツハイマー病のリスクの高い患者ではダサチニブの髄液移行が確認され、現在はP2試験が進行中です。
特徴的な投与方法も注目に値します。セノリティクスは「ヒット・アンド・ラン」型の間歇投与が可能であり、連続投与を必要としません。ダサチニブの半減期は約4時間、ケルセチンは約11時間ですが、短時間の曝露で老化細胞に不可逆なアポトーシスを誘導できます。これは、従来の一般的な医薬品とは異なる創薬モデルを示唆しています。
ただし、ダサチニブ+ケルセチンのセノリティクスには商業的な課題があります。いずれも既存薬であり特許保護がないため、大規模臨床試験に数億ドルを投じても投資回収が困難です。臨床試験は小規模にとどまり、創薬パイプラインとしてのスケールに欠けます。概念実証の基盤としては極めて重要ですが、産業的には「次世代セノリティクス」への橋渡し役という位置付けになるでしょう。
次世代セノリティクス
Unityの教訓とダサチニブ+ケルセチンの限界を踏まえ、新たなアプローチが台頭してきています。特に注目すべきは、疾患特異的な適応症から参入する戦略を採る企業群です。
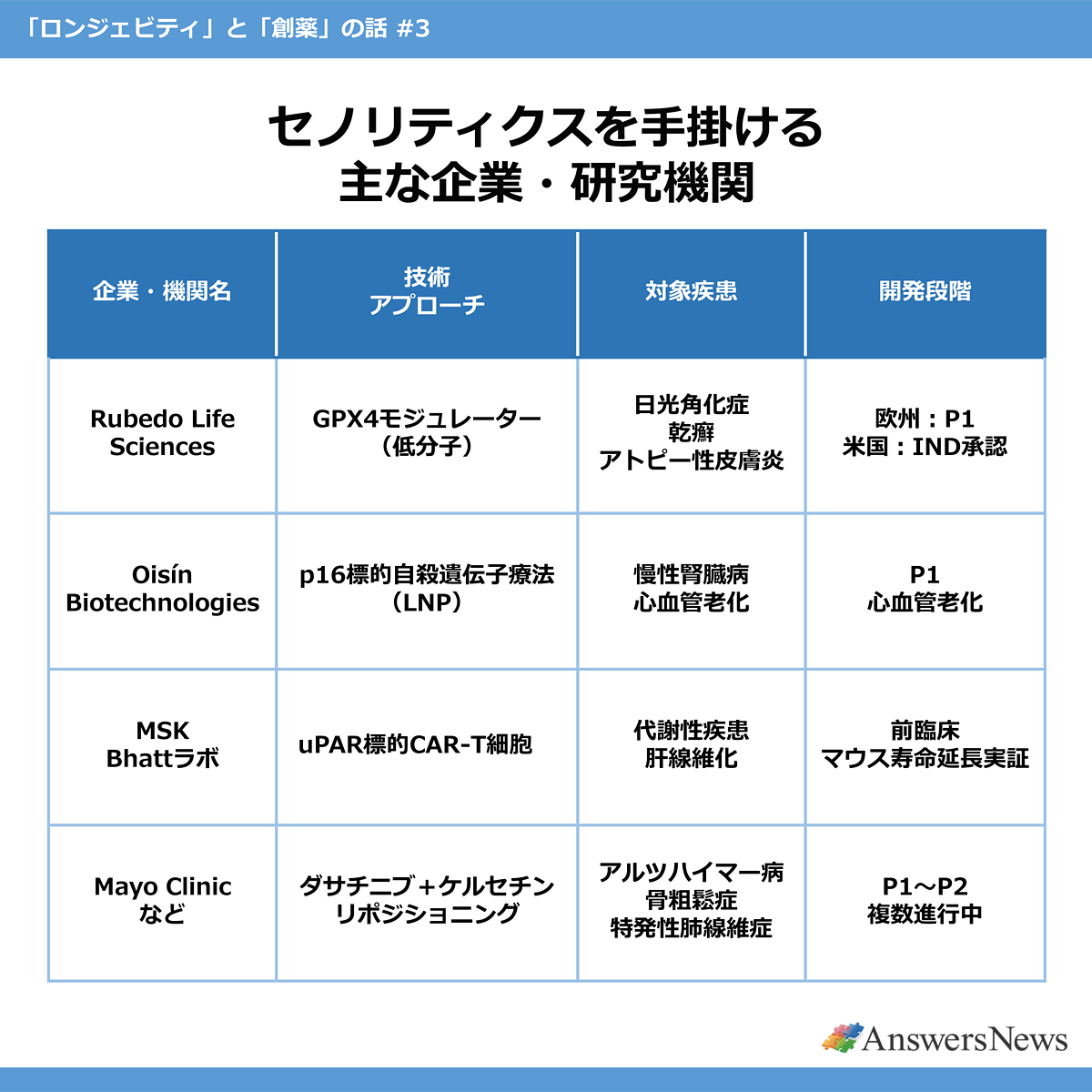
米Rubedo Life Sciencesは、2025年に最も具体的な進捗を見せた企業の1つです。同社のリード化合物「RLS-1496」は、老化細胞がアポトーシスに抵抗するために依存するGPX4(グルタチオンペルオキシダーゼ4)を選択的にモジュレートする初の低分子薬。2025年には欧州で乾癬、アトピー性皮膚炎、光老化皮膚を対象とした臨床試験が開始され、同年には米FDA(食品医薬品局)から日光角化症を対象としたIND承認も取得しました。皮膚疾患という老化細胞の役割が明確で、局所投与が可能な領域から参入する戦略は、Unityの教訓を踏まえた合理的な選択と言えます。
一方、免疫療法型のアプローチも急速に進展しています。米Memorial Sloan KetteringのBhattらは、老化細胞表面に特異的に発現するuPAR(ウロキナーゼ型プラスミノーゲン活性化因子受容体)を標的とするCAR-T細胞療法を開発しています。2024年に科学誌「Nature Aging」に発表された加齢マウスを使った研究では、1回の投与で数カ月にわたりCAR-T細胞が体内で持続し、代謝機能の改善や運動能力の向上が示されました。2025年には腸管再生の改善も報告されています。
このCAR-Tアプローチの最大の利点は、一回投与で持続的な「監視」が可能な点です。低分子セノリティクスが「ヒット・アンド・ラン」の繰り返し投与を必要とするのに対し、CAR-Tは体内で老化細胞を継続的に排除し続ける可能性があります。ただし、加齢患者では免疫老化によりCAR-T細胞自体の増殖や持続性が低下してしまうのが課題で、最も恩恵を受けるべき高齢患者で治療が最も困難になるというパラドックスが存在します。
カギ握るバイオマーカー
セノリティクスが創薬パイプラインとして成立するためには、老化細胞負荷を定量的に測定するバイオマーカーの確立が不可欠です。前回取り上げたリプログラミングの領域ではエピジェネティック・クロックがその役割を果たしており、同様のものがセノリティクスにも必要となります。
その有望な候補として注目されているのが、T細胞におけるp16バリアント5の発現量。2025年に報告されたダサチニブ+ケルセチンの骨粗鬆症対象のP2試験では、このp16バリアントの発現が高い患者ほど薬剤への反応が良好だったことが示され、「老化細胞負荷の高い患者を選択的に治療する」というプレシジョン・ヘルスケア型のアプローチの可能性が示唆されました。SASP因子や可溶性uPARなど血漿マーカーの併用も検討されており、バイオマーカーの整備が進めばセノリティクスの臨床開発も加速するでしょう。
セノリティクスは、リプログラミングとは異なる論理で老化にアプローチします。リプログラミングが「巻き戻し」であるのに対し、セノリティクスは「除去」です。損傷した細胞を取り除くという発想は、病因を特定して、それを排除するという創薬の従来の論理――に比較的なじみやすいと言えます。
ただ、Unityの失敗が示すように、そのなじみやすさは必ずしも成功を保証しません。老化細胞は組織ごとに異質であり、全身性の除去が予期せぬ副作用をもたらす可能性もあります。さらには、「どの組織のどの老化細胞を、どのタイミングで除去するか」という問いに対し、現時点では明確な答えがありません。
とはいえ、Rubedoの皮膚疾患からの参入、ダサチニブ+ケルセチンによる概念実証の積み重ね、CAR-T細胞による持続的監視という新たなモダリティは、Unityの時代には存在しなかった選択肢です。セノリティクスは最初の走者の失敗を経て、より精密な戦略を身につけつつあります。
次回は、老化創薬のもう1つの軸である「既存経路の再定義」を取り上げます。mTOR、AMPK、代謝制御など創薬標的としてすでに確立されている経路が、ロンジェビティの文脈でどのように再解釈され得るかを検討します。
| 増井慶太(ますい・けいた)ロンジェビティ特化型VC(ベンチャーキャピタル)ASAGI Labs Ventures合同会社Managing Partner、BAIOX株式会社CEO、インダストリアルドライブ合同会社CEO。ヘルスケアやライフサイエンス領域の投資運営、M&A仲介、カンパニー・クリエーション、事業運営に従事。東京大教養学部卒業後、米系経営戦略コンサルティング企業、欧州製薬企業などを経て現職。 X:@keita_masui LinkedIn:https://www.linkedin.com/in/keita-masui/ ウェブサイト:https://alv.vc/ |
あわせて読みたい
オススメの記事
-

第一三共、26年3月期の利益下振れ…ADC供給計画見直しで損失/「レケンビ皮下注」初期療法への適応拡大、FDAが審査3カ月延長 など|製薬業界きょうのニュースまとめ読み(2026年5月8日)
-

AnswersNewsは創刊10周年を迎えました。編集長より読者の皆様へお礼とご挨拶
-

MRの転職市場、スペシャリティ領域で好調…製造やMSLも採用活発|製薬業界 今月の転職求人動向レポート(2026年4月)
-

「統合」テーマにPatient Centricityを考える2日間―5月開催「Ubie Pharma Summit 2026」の見どころ【AD】
-

mRNA専門CDMOのARCALIS、社員が語るリアルな「仕事」と「魅力」【AD】