
創薬はこれまで、がん、循環器疾患、神経変性疾患など明確に定義された疾患を標的として発展してきました。疾患には診断基準があり、臨床試験には評価項目があり、規制当局はそうした枠組みに基づいて承認を行う――。医薬品開発が長らく前提としてきたこの構造は、疾患を個別に定義し、原因を特定し、標的を定めるという発想の上に成り立っています。
では、老化はどうでしょうか。
老化は普遍的かつ連続的な現象であり、従来は治療の対象とはみなされてきませんでした。しかし近年、老化研究は質的転換を迎えています。2013年に提唱された「Hallmarks of Aging」は、老化を時間の経過ではなく、複数の分子・細胞機構の相互作用として整理しました。これを機に老化は、ゲノムの不安定性、エピジェネティックの変化、ミトコンドリアの機能不全、慢性炎症、細胞老化など、絡み合ったネットワークの結果として理解されるようになってきました。
この知見はその後、「ジェロサイエンス仮説(geroscience hypothesis)」として体系化されました。すなわち、老化の根本メカニズムに介入することで、個別の老化関連疾患を同時に遅延・予防できるという考え方です。ジェロサイエンス仮説は、ロンジェビティ・バイオテクノロジー企業(LBC=Longevity Biotechnology Company)が依拠する中核概念であり、疾患と標的が対をなす従来型の創薬パラダイムに対するオルタナティブを提示しています。
Hallmarks of Agingは2023年の改訂(Lopez-Otin et al., Cell 2023)で、ディスバイオーシス(dysbiosis=腸内細菌叢の乱れ)、マクロオートファジーの機能不全(disabled macroautophagy)、慢性炎症(chronic inflammation)の3つが独立した項目として追加され、12のホールマークに拡張されました。さらに、細胞外マトリックス(ECM)の硬化なども老化の重要な特徴として議論されています。この拡張は、老化がそれまで考えられていた以上に多層的な現象であることを示すとともに、創薬標的の候補がさらに広がったことを意味します。
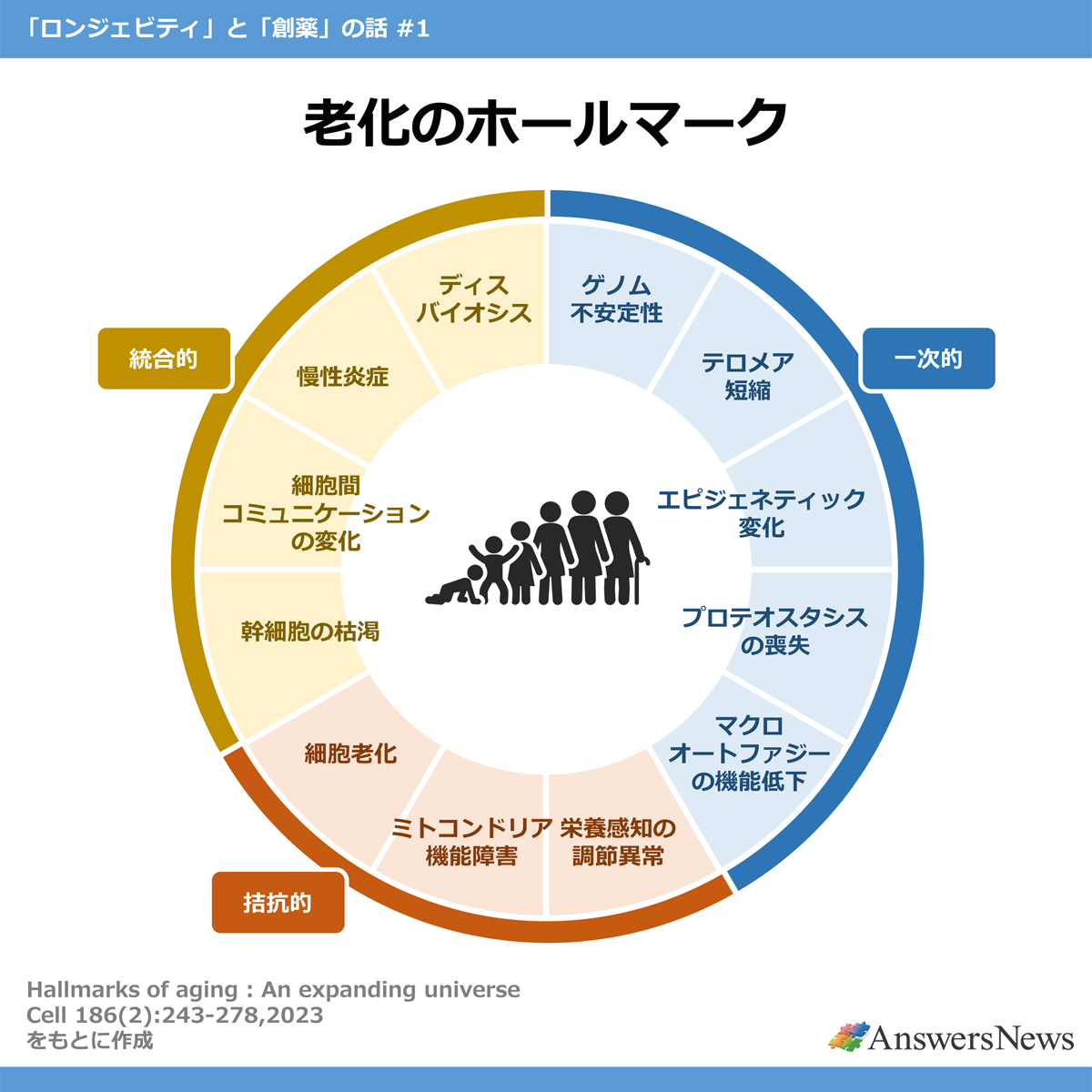
ここで押さえておかなければならないのは、老化が「分解可能」になったことを意味しているわけではないということです。ホールマークが示すのは、老化が単一標的で攻略できる単純な現象ではないという事実。エピジェネティック情報、代謝、炎症、幹細胞機能などは相互に影響し合い、生体全体の恒常性を形成しています。老化は、その調律が崩れた状態と捉える方が実態に近いと言えます。
この視点に立つと、創薬の問いは変わります。すなわち「どの標的をつぶすか」ではなく「どの介入が全体のバランスを再構築し得るか」です。
エピジェネティック・リプログラミング療法が臨床試験に
2026年1月、この問いの転換を象徴する動きがありました。米Life Biosciencesが開発する「ER-100」の米国でのIND承認です。ER-100は、AAVベクターを使ってOSK(OCT4、SOX2、KLF4の3つの転写因子)を導入し、細胞を部分的に初期化するエピジェネティック・リプログラミング療法。OSKは「山中4因子」から腫瘍化リスクの高いc-Mycを除いたもので、安全性を確保しながら老化した細胞の機能回復を狙います。治験は視神経症という明確な疾患が対象ですが、背後にあるのは、エピジェネティック情報の乱れを調整することで組織機能を整えるという発想です。
重要なのは、ER-100が「老化を治療する薬」として治験の承認を得たわけではない点です。あくまで視神経症への介入であり、老化そのものは適応症ではありません。しかし、このIND承認は、老化を構成する機構の一部に介入することでシステムの再調律を試みるアプローチが臨床段階に入ったことを意味します。
現在、老化は制度上、疾患とはされません。老化を単独の適応症として定義し、医薬品を開発するには、明確な診断基準、評価指標、臨床エンドポイントが必要となります。老化は連続的かつ個体差の大きい現象であり、現在の規制の枠組みにそのまま適合するものではありません。科学と制度の間には深い溝が横たわっています。
現実的な戦略は、老化関連疾患からのアプローチです。視神経症、加齢黄斑変性、線維化疾患、変形性関節症など老化と強く関連する疾患を適応症とし、老化機構への介入が疾患アウトカムを改善することを示すのです。しかしその場合も、単一の標的を最適化するという従来型の創薬の考え方では限界があります。老化は複雑系であり、単独経路の修復が全体の機能回復に直結するとは限らないからです。
ここに、老化をターゲットした創薬の産業的な難しさと、可能性に関する違和感があります。
従来のブロックバスターモデルは「単一疾患」「単一標的」「明確なエンドポイント」を前提としてきました。しかし、老化を対象とするなら、複数経路にまたがる統合的な介入、あるいは段階的な調律が必要になる可能性があります。このことは、創薬パイプラインの設計思想そのものを揺さぶります。
ER-100のIND承認は、老化が直ちに適応症になることを意味するわけではありませんが、創薬のタネとして臨床現実に接続し始めたことを示しています。そのタネは、従来の単一標的型の延長線上で芽吹くのでしょうか。それとも、複雑系への統合的アプローチという新しい創薬思想へとつながっていくのでしょうか。
次回以降、「エピジェネティック・リプログラミング」「老化細胞除去」「代謝制御」「AI創薬」などの具体例を見ながら、老化創薬の実現可能性を検討していきます。
| 増井慶太(ますい・けいた)ロンジェビティ特化型VC(ベンチャーキャピタル)ASAGI Labs Ventures合同会社Managing Partner、BAIOX株式会社CEO、インダストリアルドライブ合同会社CEO。ヘルスケアやライフサイエンス領域の投資運営、M&A仲介、カンパニー・クリエーション、事業運営に従事。東京大教養学部卒業後、米系経営戦略コンサルティング企業、欧州製薬企業などを経て現職。 X:@keita_masui LinkedIn:https://www.linkedin.com/in/keita-masui/ |











