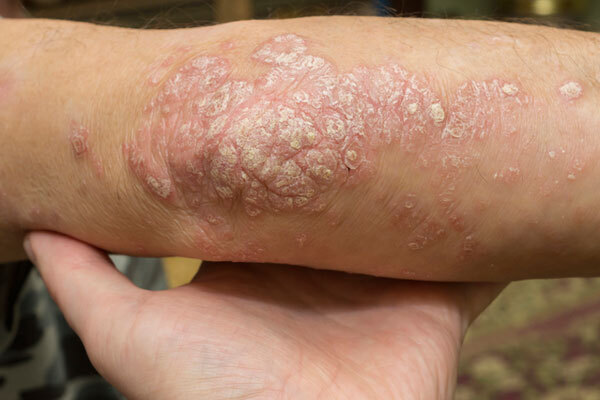
大塚ホールディングス(HD)が、次世代コア領域として自己免疫疾患への攻勢を強めています。2018年の米ビステラ、24年の同ジュナナ買収で獲得した創薬基盤を活かしてパイプラインを拡大。今年に入ってからも2つの抗体医薬を導入し、現在8つの新薬候補を開発段階に揃えています。
「腎領域とのつながりの中で検討」
「いきなり自己免疫疾患が出てきたわけではなく、腎領域とのつながりの中で注力領域として検討してきた」。大塚HDの井上眞社長CEO(最高経営責任者)は、自己免疫疾患領域への同社の取り組みについてこう話します。腎領域の常染色体優性多発性のう胞腎(ADPKD)治療薬「ジンアーク」(一般名・トルバプタン)で培ったスペシャリティ事業のノウハウを軸に、自己免疫領域を2034年以降の成長を支えるコア領域に育てる考えです。
ジンアークが特許切れを迎える中、大塚HDは次の成長ドライバーとして、精神・神経領域のウロタロントやがん領域のジパレルチニブなど「ネクスト8」と呼ぶ後期開発品の開発に注力。さらにその先も見据え、精神展開剤(サイケデリックス)や次世代ADC(抗体薬物複合体)などを取り込んでコア領域の深化を図るとともに、コア領域の幅を広げる動きをとっています。
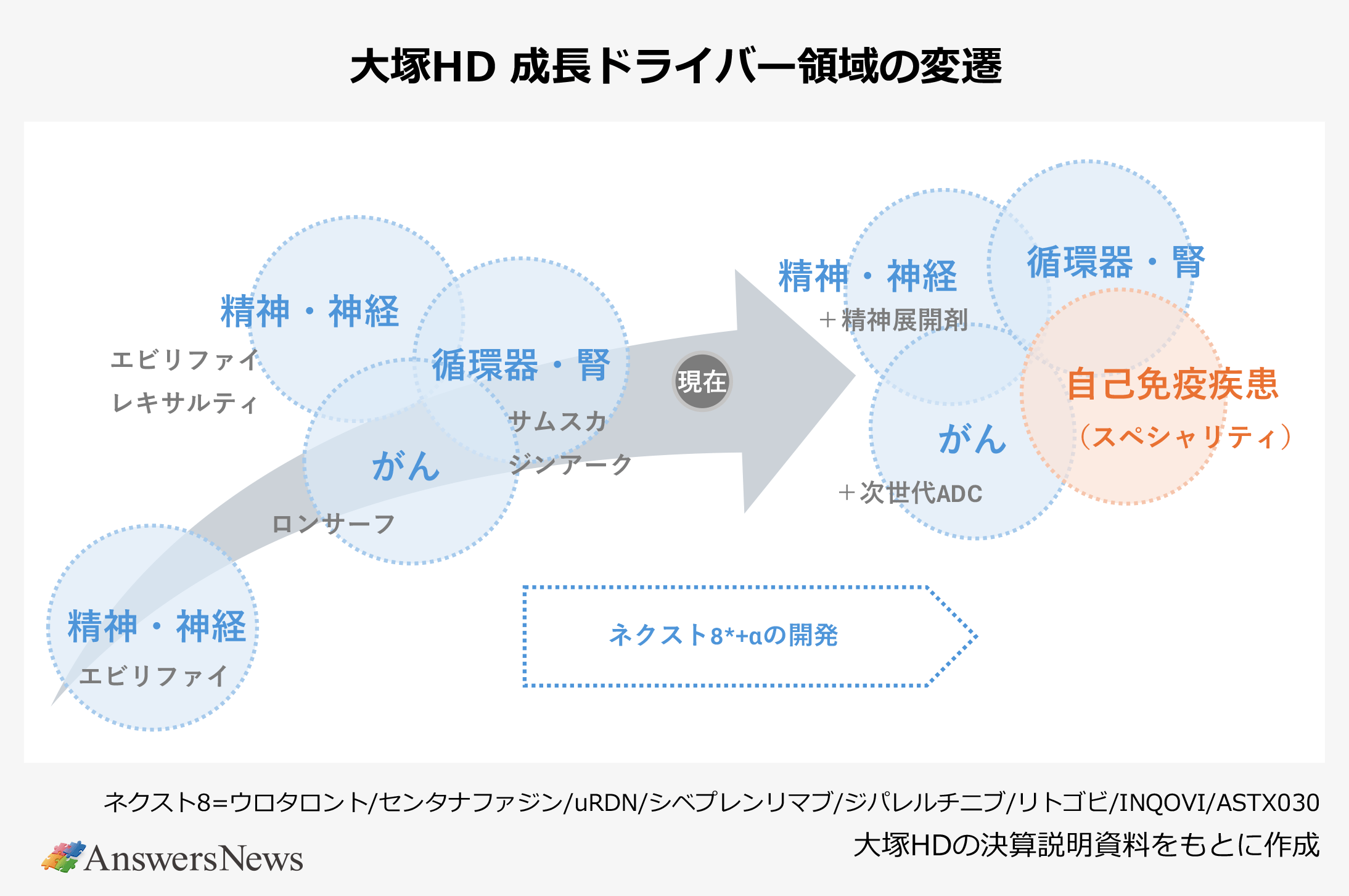
自己免疫疾患に注力する大きな契機となったのが、腎領域の強化と抗体創薬基盤の獲得を目的にして行った18年の米ビステラ買収です。これにより、同社のリードパイプラインであるAPRIL中和抗体シベプレンリマブのほか、開発の早期段階にあった複数の自己免疫疾患治療薬候補を取得。以来、大塚HDは米国の臨床開発チームの自己免疫領域のケイパビリティを強化してきました。シベプレンリマブはIgA腎症の適応で今年3月に米国で申請しており、順調にいけば11月末までの承認取得を見込んでいます。
24年の米ジュナナ買収でも低分子の自己免疫疾患治療薬候補を獲得。今年6月には、中国のハーバー・バイオメッドから自己免疫疾患に対するT細胞エンゲージャー(TCE)「HBM7020」のライセンスを取得し、翌月にはスウェーデン・カンタルジアからIL-1RAP抗体「CAN10」の関連資産を買収しました。
買収やライセンス契約でパイプライン拡大
HBM7020は、BCMAとCD3を標的とする二重特異性のTCEで、ハーバー・バイオメッドが独自技術を使って開発。自己抗体を産生するB細胞を活性化したT細胞で攻撃することで治療効果を期待します。
大塚製薬の渡邊武事業開発部長は、TCEによる治療を「切れ味の鋭いアプローチ」と評価。TCEは血液がんを中心に実用化されてきましたが、サイトカイン放出症候群などT細胞の過剰な活性化による有害事象リスクの懸念があり、自己免疫疾患での実用化例はありません。HBM7020は、従来のTCEと比べてT細胞との親和性が低く抑えられている一方、2価のBCMA結合部位を配置することで形質細胞との結合性を高めているのが特徴。大塚は、外来投与も含め、安全で簡便な治療が期待できるとみています。
一方、CAN10が標的とするIL-1RAPは、炎症性サイトカインであるIL-1、IL-33、IL-36のシグナル伝達に共通して関与するする分子。IL-1RAPを阻害することで複数のシグナル伝達経路を同時に遮断することができると期待されています。
複数のサイトカインが関わる非臨床疾患モデルでは、個々のサイトカインを阻害するよりも高い効果が確認されているといい、渡邊氏は「複数のサイトカインが関与する疾患への適応が差別化につながる」と説明。通常、抗体は合剤化しづらく、マルチな阻害作用を持つことにメリットがあると強調します。
CAN10は関連資産ごと譲り受けており、開発戦略は大塚が単独で決めていく方針。現在の臨床第1相(P1)試験は乾癬が対象ですが、P2試験ではバスケット試験を導入し、スペシャリティ疾患という視点も軸に全体方針とも照らしながら適応症を見極めていく考えです。
研究は「抗体でベストイン、低分子でファーストイン」
大塚の自己免疫疾患のパイプラインには現在、シベプレンリマブと今年に入って新たに獲得した2つのアセットを含め、8つの新薬候補が並びます。このうち、ビステラ由来の抗体医薬はシベプレンリマブを含めて4品目、ジュナナ由来の低分子薬は2品目です。
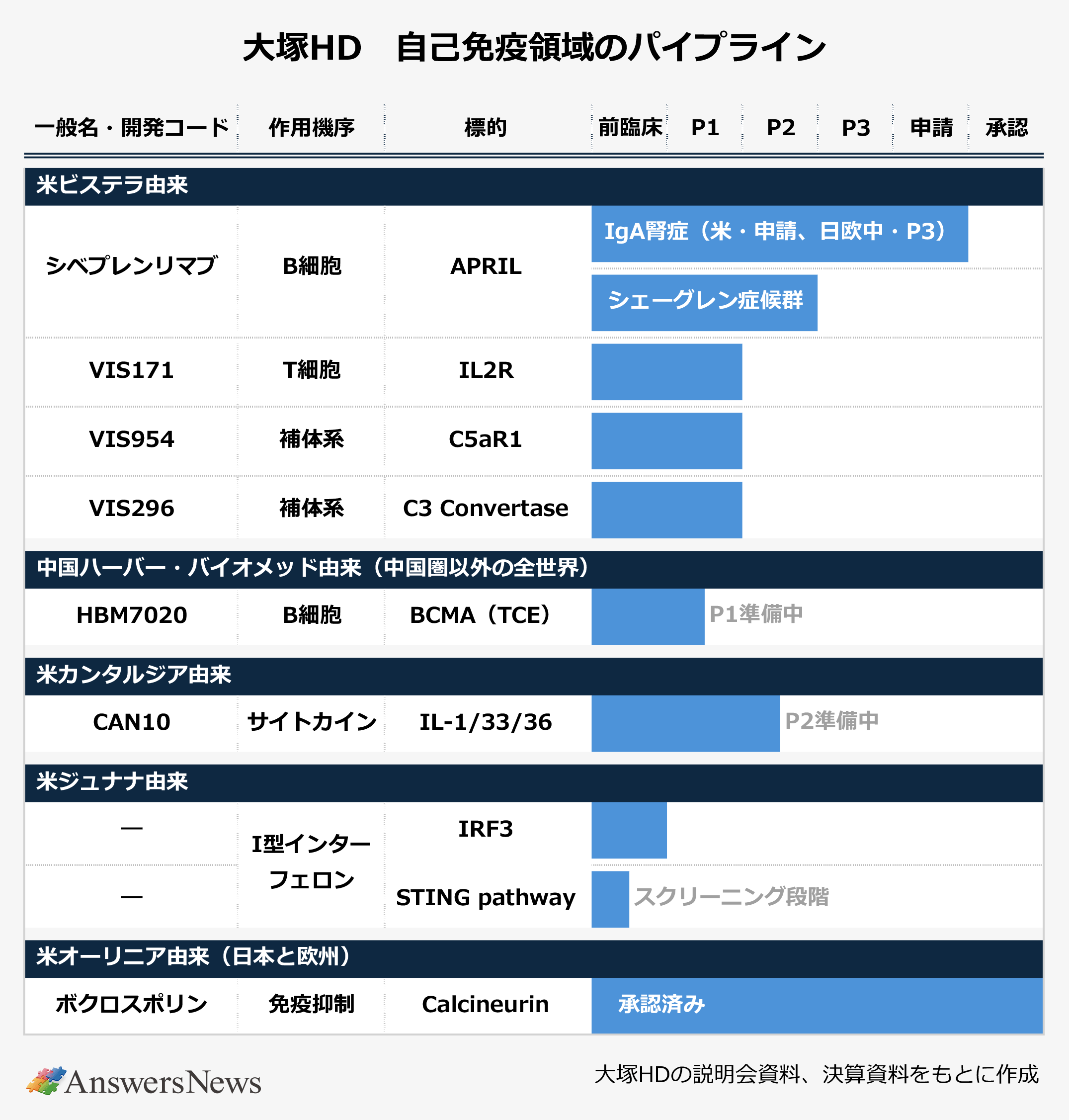
渡邊氏は自己免疫疾患領域のポートフォリオについて、「LCM(ライフサイクルマネジメント)ポテンシャルの高いものに限ってパイプライン化している」と言います。シベプレンリマブが申請中のIgA腎症を含め、各パイプラインは小型~中型の適応症で開発していく方針で、腎臓領域のほかに膠原病、皮膚疾患などが候補。小回りの利くパイプラインとすることで、「研究開発投資のタイミングと量、得られる結果のバランスを適宜経営側で意思決定できる」と渡邊氏は強調します。
28年までの現中期経営計画中の承認を見込む自己免疫疾患領域の新薬はシベプレンリマブのみで、当面は同薬と日欧で展開するループス腎炎治療薬「ルプキネス」(ボクロスポリン)がこの領域を牽引します。これらに続くビステラのパイプラインは29~33年に、それ以外の4品目は35年ごろの承認を見込んでおり、2030年ごろに複数のPOC取得を予定。将来的な売り上げは明らかにしていませんが、ピーク時予測1000億円超のシベプレンリマブに次いで期待が高いのはHBM7020とみられます。
ビステラやジュナナの新たなパイプライン創出にも期待しており、抗体医薬でのベストインクラス創出と、低分子でのファーストインクラス創出を両輪にさらなるポートフォリオ拡充を目指します。
競争の激しい抗体医薬の中核は、抗原の中のリジットな構造(標的エピトープ)に対して抗体を作るビステラのアプローチ。これを活かしたシベプレンリマブについて渡邊氏は、「APRILへの結合性が現在の後期開発品の中で最も強く、皮下注にできる高い溶解性と製造のしやすさも兼ね備えている」と自信を見せます。ビステラでは、同薬には適用していない独自の半減期延長技術を確立しているほか、次世代のTCEの開発にも着手済み。HBM7020の導入とほぼ同時期にハーバー・バイオメッドと抗体技術に関するライセンス契約も結んでおり、自己免疫疾患で開発を加速します。
一方、低分子では転写因子など細胞内の難創薬標的タンパク質に対するジュナナの技術を活用。同社はフラグメント創薬とHTS(ハイスループットスクリーニング)創薬をかけ合わせたアプローチを有しており、フラグメント創薬のパイオニアである大塚の子会社アステックスとの連携も開始しました。