(写真:ロイター)
2026年3月に米FDA(食品医薬品局)が承認した主な新薬と適応拡大を、領域別にまとめました。
INDEX
【新薬】重症白血球接着不全症に対するex vivo遺伝子治療「Kresladi」など
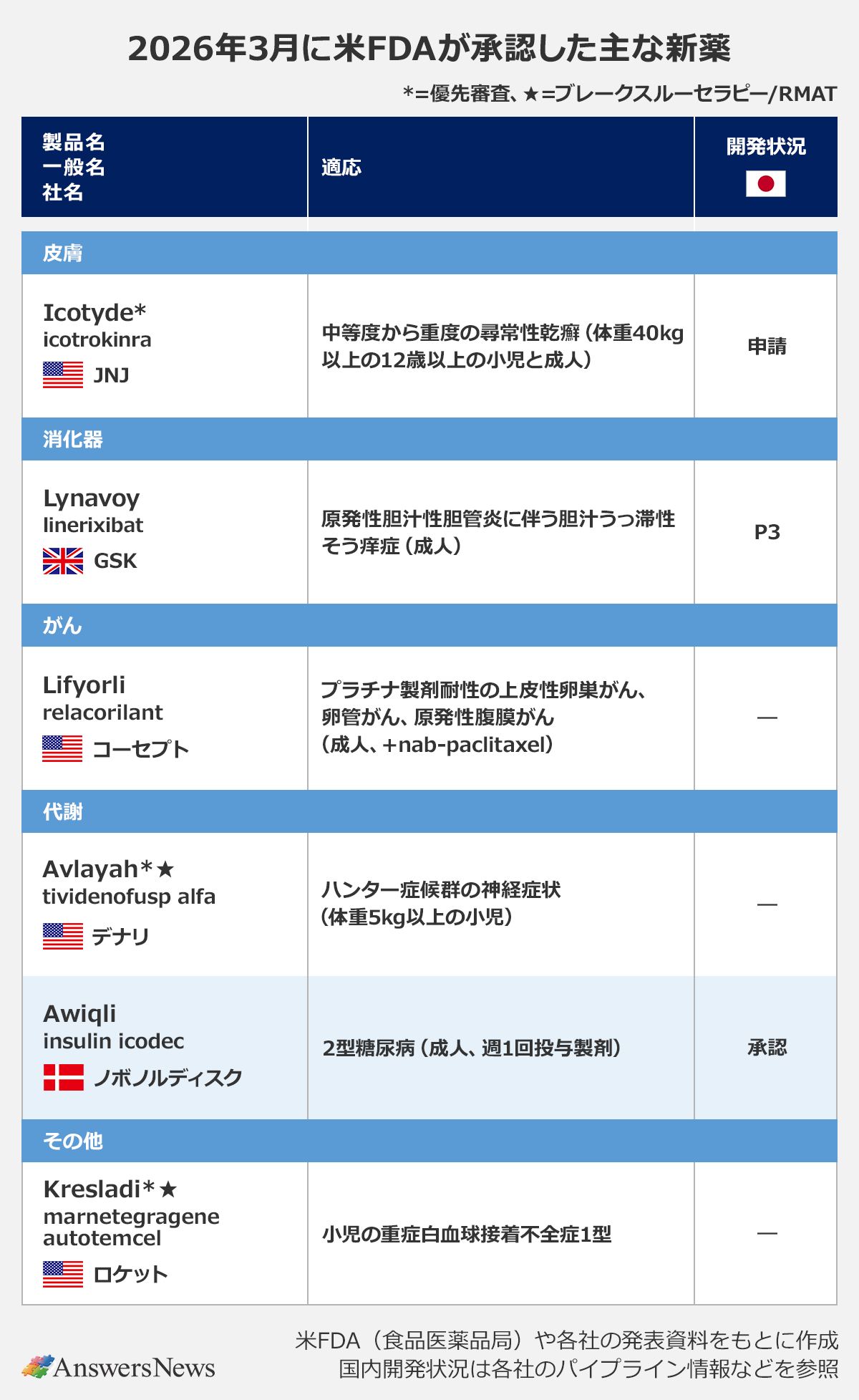
皮膚
Icotyde|米ジョンソン・エンド・ジョンソン
「Icotyde」(一般名・icotrokinra)は、中等度から重度の尋常性乾癬に対する治療薬。全身療法や光線療法の候補となる体重40kg以上・12歳以上の患者が対象です。同薬はIL-23受容体を選択的に阻害する経口ペプチド。臨床試験では1日1回の服用で皮膚病変の改善を示し、直接比較でTYK2阻害薬「Sotyktu」(deucravacitinib)に対する優越性も確認されました。日本と欧州でも申請中です。
関連記事(日本国内の状況):レッドオーシャンの乾癬治療薬市場、新たな経口薬が相次ぎ登場へ…ヤンセンが経口ペプチド申請、武田と科研は新規TYK2阻害薬
消化器
Lynavoy|英グラクソ・スミスクライン
回腸胆汁酸トランスポーター(IBAT)阻害薬「Lynavoy」(linerixibat)は、原発性胆汁性胆管炎(PBC)に伴う胆汁うっ滞性そう痒症に対する米国初の治療薬。胆汁うっ滞性そう痒はPBC患者の最大89%が経験するとされます。欧州や中国でも申請中で、日本では臨床第3相(P3)試験の段階。承認取得直前の3月9日、GSKは同薬の全世界の権利を伊アルファシグマに供与することを発表しています。
がん
Lifyorli|米コーセプト・セラピューティクス
選択的グルココルチコイド受容体拮抗薬「Lifyorli」(relacorilant)は、成人のプラチナ製剤耐性の上皮性卵巣がん、卵管がん、原発性腹膜がんの治療薬。抗VEGF抗体bevacizumabを含む1~3つの全身療法を受けた患者が対象で、nab-paclitaxelと併用します。381人を対象に行った臨床試験では、nab-paclitaxel単独と比べて死亡リスクを35%低減しました。
代謝
Avlayah|米デナリ・セラピューティクス
「Avlayah」(tividenofusp alfa)は、ライソゾーム疾患のハンター症候群(ムコ多糖症II型)に対する酵素補充療法。患者47人を対象に行ったP1/2試験の結果に基づいて迅速承認されました。血液脳関門(BBB)を通過するハンター症候群治療薬は米国初となります。
Awiqli|デンマーク・ノボノルディスク
「Awiqli」(insulin icodec)は、米国初の週1回投与のインスリン製剤。成人の2型糖尿病を対象に承認されました。日本や欧州では24年に承認を取得しています。
その他
Kresladi|米ロケット・ファーマシューティカルズ
「Kresladi」(marnetegragene autotemcel)は、ITGB2遺伝子の両アレル変異を原因とする重症白血球接着不全症1型の治療薬。患者の造血幹細胞にITGB2遺伝子を含むベクターを導入するex vivo遺伝子治療で、同種造血幹細胞移植の血縁ドナーがいない小児患者に使用されます。好中球表面のCD18とCD11aの発現上昇と効果の持続が認められた臨床試験の結果をもとに迅速承認を取得しました。繰り返す感染症と高い死亡率で知られる同疾患の根本原因にアプローチする新薬として期待されています。
【適応拡大】TecvayliとDarzalex FASPROの併用療法承認など
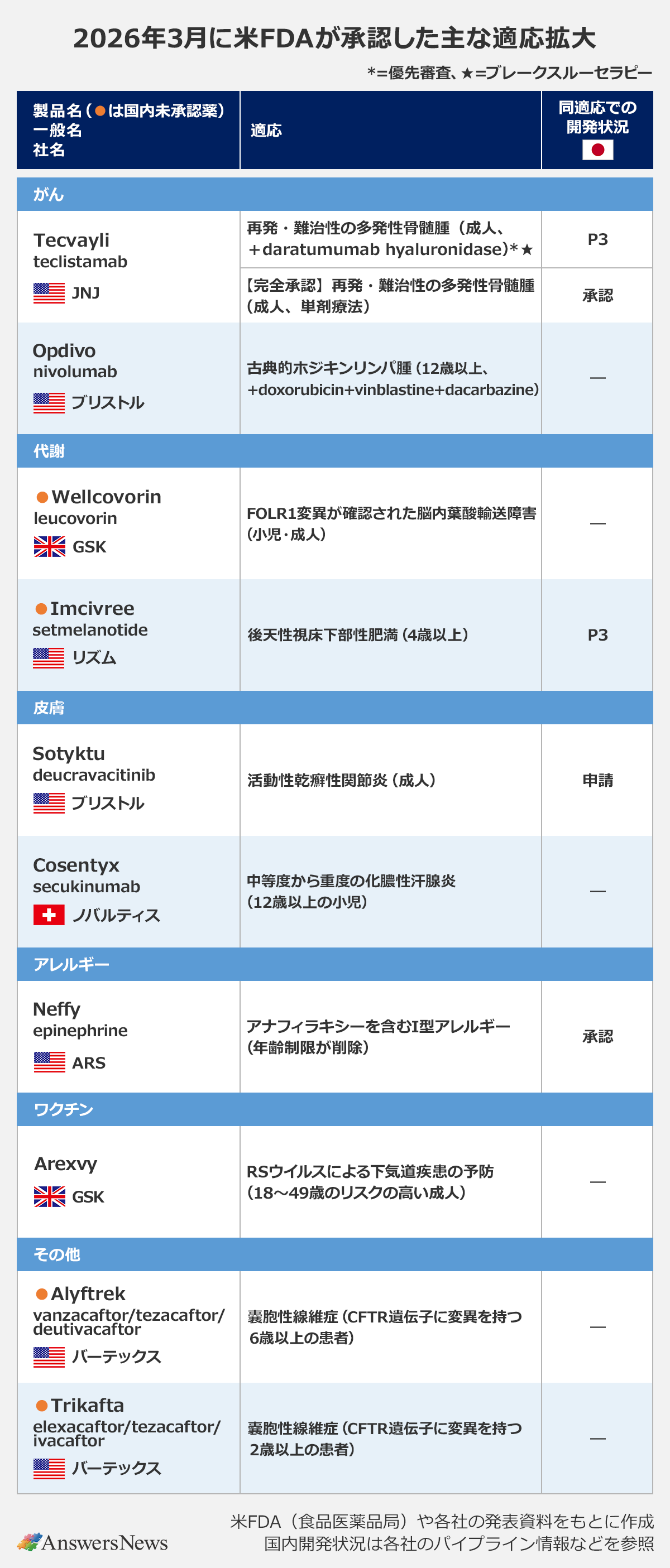
がん
Tecvayli|米ジョンソン・エンド・ジョンソン
抗BCMA/CD3二重特異性抗体「Tecvayli」(teclistamab)は、成人の再発・難治性の多発性骨髄腫の適応で抗CD38抗体「Darzalex FASPRO」(daratumumab hyaluronidase)との併用療法の承認を取得しました。プロテアソーム阻害薬と免疫調整薬を含む1つ以上の前治療を受けた患者が対象です。P3試験では、標準治療と比べて病勢進行・死亡のリスクを83%低下させました。同試験には日本も参加しています。あわせて、22年に迅速承認されたTecvayliの単剤療法は完全承認されました。
Opdivo|米ブリストル・マイヤーズスクイブ
抗PD-1抗体「Opdivo」(nivolumab)は、抗がん剤doxorubicin、vinblastine、dacarbazine(AVD)との併用療法が、未治療のステージⅢまたはⅣ期の古典的ホジキンリンパ腫の適応で新たに承認されました。12歳以上の患者を対象に行った臨床試験では、AVDと抗CD30抗体薬物複合体brentuximab vedotinの併用療法と比べて無増悪生存期間を有意に改善。欧州でも同試験をもとに申請を行っています。
代謝
Wellcovorin|英グラクソ・スミスクライン
抗葉酸代謝拮抗薬「Wellcovorin」(leucovorin)は、FOLR1変異が確認された脳内葉酸輸送障害に適応拡大しました。まれな遺伝性疾患で、脳の健康に不可欠な葉酸が不足し、重度の発達遅延や運動障害を伴います。同疾患への治療薬は米国初となります。
Imcivree|米リズム・ファーマシューティカルズ
MC4受容体作動薬「Imcivree」(setmelanotide)は、後天性視床下部性肥満(HO)に適応拡大。HOは視床下部の異常で食欲や代謝が乱れて急激な体重増加を引き起こす疾患で、同疾患の治療薬は米国初。臨床試験では、プラセボと比べてBMIを有意に減少させました。日本でもP3試験の段階にあり、今後、申請が行われる見通しです。
皮膚
Sotyktu|米ブリストル・マイヤーズスクイブ
TYK2阻害薬「Sotyktu」(deucravacitinib)は、成人の活動性乾癬性関節炎(PsA)に適応拡大。P3試験ではプラセボと比べて有意に高いACR20(関節リウマチ治療の評価基準)改善率を示しました。日本でも同適応への適応拡大を申請中です。
Cosentyx|スイス・ノバルティス
抗IL-17A抗体「Cosentyx」(secukinumab)は、中等度から重度の化膿性汗腺炎の適応で12歳以上の小児に対象を拡大。成人では23年に承認されていました。同疾患は患者の半数以上が思春期に発症するため、早期の治療介入の重要性が指摘されていました。
アレルギー
Neffy|米ARSファーマシューティカルズ
epinephrine点鼻スプレーの「Neffy」は、添付文書の年齢制限を削除。体重33ポンド(約15kg)以上の小児と成人のアナフィラキシーを含むI型アレルギーの緊急治療に使用できるようになりました。従来は、4歳以上に限られていました。日本では導入したアルフレッサファーマが今年2月に発売しています。
ワクチン
Arexvy|英グラクソ・スミスクライン
RSウイルスワクチン「Arexvy」は、18~49歳の高リスクの成人に対象を拡大。米国では60歳以上を対象に23年、50~59歳を対象に24年に承認されていました。49歳以下の成人に対しては、60歳以上との比較で免疫応答の非劣性を示したP3試験の結果に基づいて承認。日本でも18~49歳への適応拡大を申請中です。
その他
Alyftrek/Trikafta|米バーテックス・ファーマシューティカルズ
嚢胞性線維症治療薬「Alyftrek」(vanzacaftor/tezacaftor/deutivacaftor)は、臨床データやin vitroデータに基づいて反応性があるか、CFTRタンパク質の産生を伴うCFTR遺伝子変異を1つ以上有する6歳以上の患者に対象を拡大。CFTRタンパク質の産生につながるあらゆる変異が適応となり、米国では患者の95%が同薬の治療対象となりました。同「Trikafta」(elexacaftor/tezacaftor/ivacaftor)も、2歳以上の患者を対象に同様の対象拡大が認められました。
【バイオシミラー】テバのdenosumab

Ponlimsi|イスラエル・テバファーマシューティカルズ
骨粗鬆症治療薬「Ponlimsi」は、抗RANKL抗体「Prolia」(denosumab)のバイオシミラー。同薬のバイオシミラーは米国で10剤目。欧州でも承認済みです。