(写真:ロイター)
2026年2月に米FDA(食品医薬品局)が承認した主な新薬と適応拡大を、領域別にまとめました。
【新薬】週1回投与の軟骨無形成症薬「Yuviwel」など

代謝
Loargys|スウェーデン・イムメディカファーマ
ヒトアルギナーゼ1酵素製剤「Loargys」(一般名・pegzilarginase)は、アルギナーゼ1欠損症に伴う高アルギニン血症を対象に、タンパク質制限との併用療法が迅速承認されました。アルギナーゼ1の欠損は、血漿アルギニンやその毒性代謝物の蓄積を引き起こします。臨床試験では、血漿アルギニン値を迅速かつ持続的に低下させることが確認されました。欧州でも23年に承認済みです。
Desmoda|米エトン・ファーマシューティカルズ
中枢性尿崩症治療薬「Desmoda」はdesmopressin acetateの経口液。既存薬は錠剤で、患者ごとに投与量を調整するために分割や粉砕を行う必要がありました。経口液の承認により投与量の管理がしやすくなると期待されています。
精神
Bysanti|米ヴァンダ・ファーマシューティカルズ
抗精神病薬「Bysanti」(milsaperidone)は、双極性障害I型の躁病または混合性エピソードの急性期と、統合失調症の1次治療を対象に承認されました。同薬は経口投与されるとiloperidoneに変換され、ドパミンD2やセロトニン5-HT2A、α1アドレナリン受容体に拮抗することで効果を発揮します。臨床試験では、治療用量スペクトラム全体にわたるiloperidoneとの生物学的同等性が示されました。
皮膚
Adquey|米アクロテック・バイオファーマ
「Adquey」(difamilast)は、軽症から中等症のアトピー性皮膚炎治療薬。2歳以上の小児と成人が対象です。同薬は大塚製薬が創製したPDE4阻害薬で、日本では「モイゼルト」の製品名で承認されています。21年に米Acrotech Biopharmaに米国でのライセンスが供与されました。
その他
Yuviwel|デンマーク・アセンディスファーマ
週1回投与のC型ナトリウム利尿ペプチド「Yuviwel」(navepegritide)は、2歳以上の小児の軟骨無形成症の治療薬として迅速承認を取得。独自技術で長時間作用を実現しており、治療負担の軽減が期待されます。日本では帝人ファーマが臨床第3相(P3)試験を実施中です。
【適応拡大】「Keytruda」の卵巣がんなど
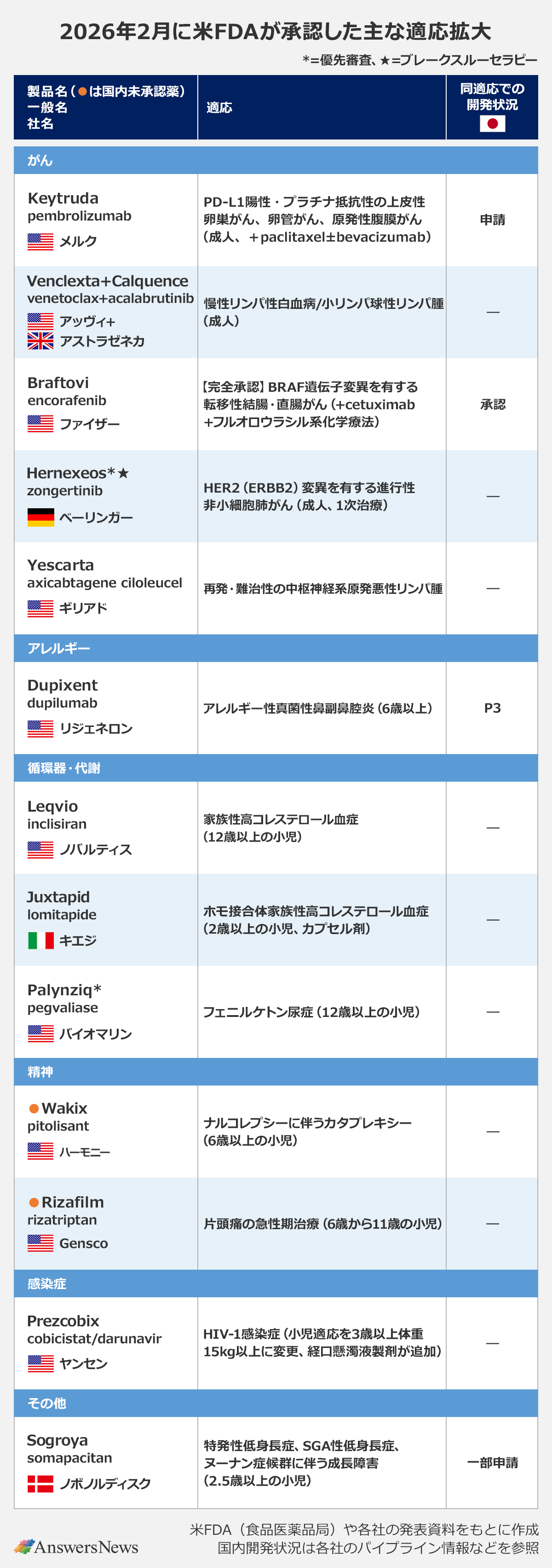
がん
Keytruda|米メルク
抗PD-1抗体「Keytruda」(pembrolizumab)は、PD-L1陽性のプラチナ抵抗性の上皮性卵巣がん、卵管がん、原発性腹膜がんの適応で承認されました。対象は1つ~2つの全身療法を受けた患者で、抗がん剤paclitaxelと併用します。皮下注製剤も同適応で承認されました。P3試験では、paclitaxelとプラセボの併用と比べて、進行または死亡のリスクを28%、死亡のリスクを24%低減させました。日本と欧州でも卵巣がんの適応で申請中です。
Venclexta+Calquence|米アッヴィ+英アストラゼネカ
BCL2阻害薬「Venclexta」(venetoclax)とBTK阻害薬「Calquence」(acalabrutinib)の併用療法は、慢性リンパ性白血病と小リンパ球性リンパ腫の適応で未治療患者への使用が承認されました。両疾患の未治療患者に対する経口薬のみ・投与期間固定の併用レジメンは初。P3試験では、化学免疫療法と比べて進行または死亡のリスクを35%低減しました。
Braftovi|米ファイザー
BRAF阻害薬Braftovi(encorafenib)は、BRAF V600E遺伝子変異を有する転移性結腸・直腸がんの適応で、抗EGFR抗体cetuximabとフルオロウラシル系化学療法との併用療法の完全承認を取得しました。同適応では24年、P3試験の全奏効率をもとに迅速承認を取得。同試験で、化学療法に対して無増悪生存期間と全生存期間の有意かつ臨床的に意義のある改善が確認されたとして完全承認に至りました。日本では昨年11月に適応拡大が承認されています。
Hernexeos|独ベーリンガーインゲルハイム
HER2阻害薬「Hernexeos」(zongertinib)は、HER2(ERBB2)チロシンキナーゼドメイン変異を有する進行性非小細胞肺がんを対象に、1次治療として迅速承認を取得。承認の根拠となったP1b試験の未治療患者コホートの客観的奏効率は76%で、患者の64%で6カ月以上の奏効持続期間を示しました。既治療患者に対しては、昨年8月に米国で迅速承認を取得。日本でも既治療患者を対象に昨年9月に承認されています。
Yescarta|米ギリアド・サイエンシズ
CAR-T細胞療法「Yescarta」(axicabtagene ciloleucel)は、再発・難治性の中枢神経系原発悪性リンパ腫に使用できるようになりました。米ダナ・ファーバーがん研究所が行った医師主導P1治験の結果に基づき、添付文書で再発・難治性大細胞型B細胞リンパ腫の適応に付記されていた使用制限の記述が削除されました。
アレルギー
Dupixent|米リジェネロン・ファーマシューティカルズ
抗IL-4/IL-13受容体抗体「Dupixent」(dupilumab)は、アレルギー性真菌性鼻副鼻腔炎に適応拡大しました。対象は、副鼻腔手術を受けた6歳以上の小児と成人。同疾患は手術を必要とすることが多く、術後の再発率が高いことが知られています。P3試験では、プラセボとの比較で症状を軽減し、全身性ステロイドの使用と手術の必要性を減少させました。日本ではP3試験が進行中です。
循環器・代謝
Juxtapid|伊キエジ
MTP阻害薬「Juxtapid」(lomitapide)は、ホモ接合体家族性高コレステロール血症の適応で2歳以上の小児に対象を拡大。小児に使用するカプセル剤も承認されました。食事療法やほかのLDL-コレステロール低下治療と組み合わせて使用します。成人向けには12年に承認されています。
Palynziq|米バイオマリン・ファーマシューティカルズ
フェニルケトン尿症に対する酵素補充療法「Palynziq」(pegvaliase)は、12歳以上の小児に対象を拡大しました。承認の根拠となったP3試験では、食事療法のみと比べて血中フェニルアラニン濃度を有意に低減しました。成人向けには米国で18年に、日本で23年に承認されています。
精神
Wakix|米ハーモニー・バイオサイエンシズ
ヒスタミンH3受容体拮抗薬/逆作動薬「Wakix」(pitolisant)は、ナルコレプシーに伴うカタプレキシーの適応で、6歳以上の小児を対象に追加しました。これにより、ナルコレプシーに伴う日中の過度な眠気とカタプレキシーの両方で小児と成人に使用できるようになりました。日本では、ヴィアトリス製薬が昨年末にナルコレプシーと睡眠時無呼吸症候群の治療薬として申請しています。
その他
Sogroya|デンマーク・ノボノルディスク
週1回投与の成長ホルモン製剤「Sogroya」(somapacitan)は、2歳半以降の小児の▽特発性低身長症▽2歳までにキャッチアップしていないSGA性低身長症▽ヌーナン症候群に伴う成長障害──の適応を追加しました。臨床試験では、1日1回投与との非劣性が確認されています。同薬は成長ホルモン分泌不全性低身長症治療薬として、米国で成人向けに20年、小児向けに23年に承認。日本でも同適応で承認済みで、昨年7月、SGA性低身長症とヌーナン症候群における低身長症への適応拡大を申請しました。特発性低身長症はP3段階です。
あわせて読みたい
オススメの記事
-

リリー、神戸・西神工場に200億円投資/富士フイルム、ADC技術基盤持つオーストリア企業に出資 など|製薬業界きょうのニュースまとめ読み(2026年3月12日)
-

【2025年版】製薬企業なんでもランキング―売上高・研究開発費・年収・従業員数・承認取得数
-

MR、複数の外資系企業で大型採用続く…研究や製造は新薬大手でピンポイントの募集|製薬業界 今月の転職求人動向レポート(2026年2月)
-

2025年 国内新薬承認取得数ランキング…1位は10承認のヤンセンファーマ、新規有効成分も4成分でトップ
-

内資系CROのパイオニア、イーピーエスが海外事業拡大へ取り組み加速…要となる「グローバルPM」の仕事と魅力とは【AD】