3月6日、iPS細胞を使った再生医療等製品2品目が世界で初めて日本で承認されました。住友ファーマがパーキンソン病向けに開発した「アムシェプリ」と、大阪大発ベンチャー・クオリプスの心筋細胞シート「リハート」で、いずれも条件・期限付きでの承認。これらに続く製品の開発も進んでいます。京都大の山中伸弥教授らが2006年にマウスでのiPS細胞の作製成功を発表してから20年。iPS細胞を使った再生医療は実用化のフェーズに踏み出します。
承認期限は7年
住友ファーマのアムシェプリ(一般名・ラグネプロセル)は、非自己iPS細胞を分化誘導して製造した非凍結状態のドパミン神経前駆細胞で、適応症は「レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソン病患者の運動症状の改善」。患者の脳内に移植し、減少したドパミン神経細胞を補うことで運動機能の改善を図ります。
50~69歳の患者7人を対象に京都大で行った医師主導治験では、有効性評価の対象となった6人のうち4人でMDS-UPDRS(国際パーキンソン病・運動障害学会統一パーキンソン病評価尺度)のパートIII(運動症状の指標)のオフスコア(薬剤治療の効果がない時=オフ時に行った評価)の改善を確認。オフ時のHoehn and Yahr重症度分類(パーキンソン病の進行度を示す指標)も6人中4人で改善しました。
クオリプスのリハートは他家iPS細胞由来の心筋細胞シート。適応症は「薬物治療や侵襲的治療を含む標準治療で効果不十分な虚血性心筋症による重症心不全の治療」です。患者の心臓に貼り付ける形で移植すると、心臓に新たな血管が形成され、組織を修復すると考えられています。患者8人を対象に行った医師主導治験の結果に基づいて承認されました。
2製品とも承認期限は7年。その間に有効性と安全性を検証することなどが承認条件として付けられています。

山中氏「20年の節目に大きな一歩」
京都大の山中教授は、厚生労働省の部会が2製品の承認を了承した2月19日、「20年の節目に社会実装へ向けた大きな一歩を踏み出せたことを嬉しく思う」とのコメントを発表。「医療として確立するため、さらに多くの症例で安全性と有効性を確かめるプロセスが不可欠。浮足立つことなく、一歩ずつ着実に進んでいくことが重要だ」と指摘しました。
一方、かねてから日本の条件・期限付き承認制度に批判的な姿勢を示してきた英科学誌ネイチャーは同月、データ不足への懸念を伝える記事を掲載。安全性と有効性を確認するには、より大規模な試験が必要だとする研究者らの声を報じています。
承認期限内に行われる安全性・有効性の検証では、アムシェプリが35例、リハートが75例(別途、対象群として非投与の150例のデータを収集して比較)を対象とした調査を行うことが求められています。
住友ファーマ「将来的に世界で売上高10億ドル超」
住友ファーマは再生・細胞医薬を重点領域の1つに据えており、アムシェプリは現在、米国での開発が進行中。眼科領域でも他家iPS細胞由来製品を開発しており、日本ではヘリオスとともに網膜色素上皮細胞「HLCR011」の臨床第1/2相(P1/2)試験を、米国では網膜シート「DSP-3077」を使ったP1/2試験をそれぞれ進めています。
再生医療ではiPS細胞以外にも、小児先天性無胸腺症向け他家培養胸腺組織「リサイミック」を米国で展開しており、再生・細胞医療事業を30年代半ばに最大1000億円、30年代後半には最大3500億円規模の事業に育成する考え。同社の木村徹社長は2月17日に開いた研究開発に関する説明会で、アムシェプリについて「グローバルで10億ドルを超えるような製品にできるのではないか」と話しました。
クオリプスもリハートの海外開発に乗り出しています。米スタンフォード大と共同研究契約を結んでおり、治験に向けた準備を実施中。カテーテルを使った移植についても研究開発を進めています。
Heartseedは27年発売目指し開発
心不全に対しては、慶応大発ベンチャーのHeartseedが昨年、他家iPS細胞由来の心筋再生治療薬「HS-001」の国内P1/2試験で全10例の投与を終了。26年中の申請に向けてデータのとりまとめを進めており、27年の発売を目指しています。試験は虚血性心疾患に伴う重症心不全を対象に実施。低用量では5例中3例、高用量では5例中4例で改善が見られたといいます。
HS-001は、1000個程度の心筋細胞を塊にした心筋球を心臓に移植するもので、高い生着率が見込めるとしています。HS-001は冠動脈バイパス手術と同時に移植しますが、カテーテルで移植する「HS-005」についても今年前半の国内P1/2試験開始を計画。海外展開では、デンマークのノボノルディスクと提携していましたが、昨年9月、同社が再生医療から撤退したことに伴い権利を再取得。自社展開も含めて可能性を検討している段階です。
京大発ベンチャーのiHeart Japanも昨年、他家iPS細胞由来心血管系細胞多層体「IHJ-301」の国内P1/2試験を開始。拡張型心筋症の患者10人が対象です。
CAR-Tの開発も活発
心疾患以外では、阪大発ベンチャーのレイメイが2月10日、他家iPS細胞由来角膜上皮細胞シート「REM-01」の企業治験開始を発表。角膜上皮幹細胞疲弊症の患者12人の組み入れを予定します。同社にはロート製薬が出資しており、共同で製造・販売を行う方針です。
iPS細胞由来の角膜内皮代替細胞移植「CLS001」の実用化を目指す慶応大のチームも、同大発スタートアップを通じて27年の製品化に向けてP1試験を進めています。国内ベンチャーではこのほか、ケイファーマが亜急性期脊髄損傷の医師主導臨床研究を終え、27年にも企業治験を開始する計画。オリヅルセラピューティクスは同種iPS細胞由来膵島細胞シート「OATx-410」が医師主導P1試験の段階にあります。オリヅルはこの3月末で終了する武田薬品工業と京都大学iPS細胞研究所(CiRA)の10年間の共同研究から生まれたベンチャーです。
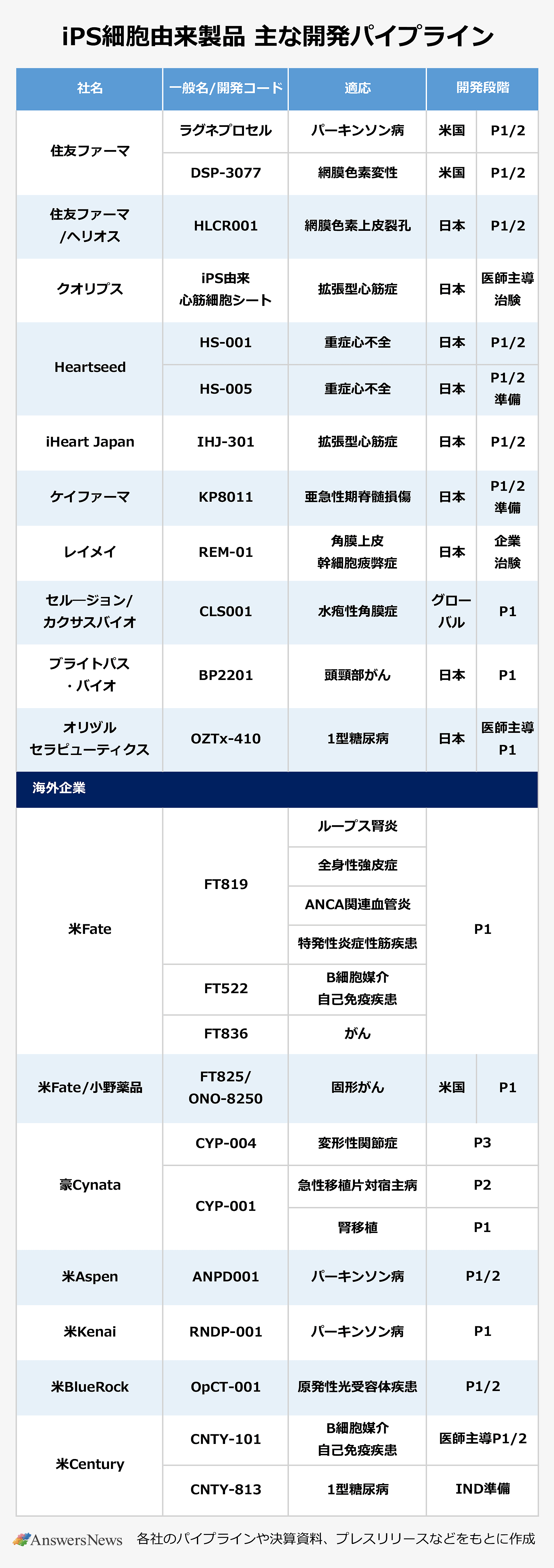
小野薬品など参入
iPS細胞から作製した免疫細胞の開発も活発です。ブライトパス・バイオは他家iPS細胞由来再生NKT細胞「BP2201」の頭頸部がんを対象としたP1試験を完了。パイプラインには他家iPS細胞由来BCMA CAR-NKT細胞療法も控えています。
小野薬品工業は米Fate TherapeuticsとiPS細胞由来のHER2 CAR-T細胞療法「ONO-8250/FT825」を共同開発。現在米国でP1段階にあります。
FateはFT825以外にも複数のiPS細胞由来CAR-T細胞の開発を進めており、リードパイプラインであるCD19標的の「FT819」はループス腎炎や全身性強皮症などがP1試験段階。iPS細胞由来CAR-NK細胞「FT522」もP1試験が進んでいます。
富士フイルムの提携先である米Century Therapeuticsは、CD19標的のiPS細胞由来CAR-iNK細胞「CNTY-101」が医師主導P1/2試験段階。同社が優先プログラムに位置付ける1型糖尿病に対する他家iPS細胞由来膵島β細胞「CNTY-813」は、早ければ今年中にIND(治験開始)申請が行われる見通しです。富士フイルムはパーキンソン病に対する「RNDP-001」を開発する米Kenai Therapeuticsとも提携を結んでいるほか、独バイエル子会社の米BlueRockに網膜疾患の原発性光受容体疾患治療薬「OpCT-001」の開発・商業化ライセンスを供与しています。










