
高リスク筋層非浸潤性膀胱がん治療に、BCGの承認以来、約40年ぶりとなる新薬が登場します。今年8月にはフェリング・ファーマが遺伝子治療薬を、9月にはヤンセンファーマが抗がん剤の局所送達システムを相次いで申請。いずれも来年の承認が見込まれます。BCG治療が奏効しない場合の治療は主に膀胱全摘除術に限られており、これらの新薬候補は膀胱を温存できる治療選択肢として期待されています。
BCG不応性にアンメットニーズ
膀胱がんは膀胱にできるがんの総称で、そのほとんどが尿路上皮と呼ばれる粘膜にできる尿路上皮がんです。深達度によって、がんが粘膜上皮や上皮化結合組織にとどまる筋層非浸潤性膀胱がんと、がんが筋層まで及んでいる筋層浸潤性膀胱がんに分類されます。
国内の膀胱がんの新規患者数は2万4448人(2021年、国立がん研究センターがん情報サービスのがん統計)で、死亡者数は9591人(23年、同)。筋層非浸潤性膀胱がんは、全膀胱がんの約7~8割を占めます。
筋層非浸潤性膀胱がんは、がんの数や大きさ、深達度、異形度、上皮内がん併発の有無などによってリスク分類されます。治療はリスク分類に応じて選択され、低リスクと中リスクの一部では細胞障害性抗がん剤を、中リスクの一部と高リスクではBCGを膀胱内に注入するのが標準的です。ただ、高リスク患者の半数以上は1年以内に再発・進行し、多くがBCGに反応しない状態へと移行。BCGが奏功しなくなった場合、治療は膀胱の全摘か臨床試験への参加に限られます。
高リスクは筋層非浸潤性膀胱がん全体の15~44%を占めますが、その治療はBCGが登場した約40年前からほとんど進展がありません。BCG不応性の治療は極めて限定的で、新たな選択肢が求められていました。
3カ月1回投与の遺伝子治療、持続的局所送達の膀胱内システム
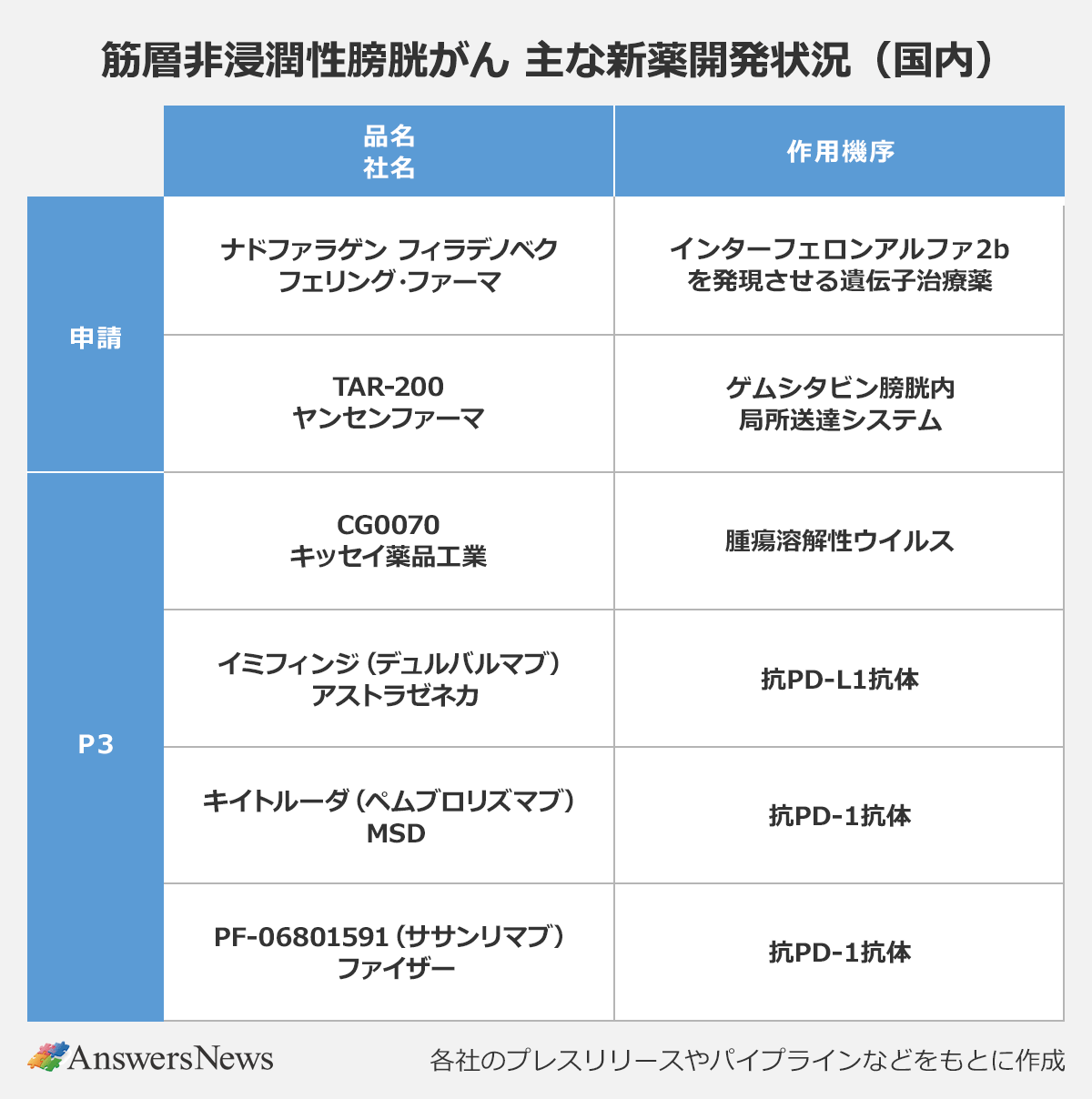
こうした中、フェリング・ファーマは8月27日、BCG治療が奏功しない筋層非浸潤性膀胱がんに対する遺伝子治療薬ナドファラゲン フィラデノベク(一般名)を申請。9月8日にはヤンセンファーマが抗がん剤ゲムシタビンの膀胱内システム「TAR-200」(開発番号)を申請しました。QOLに大きな影響を与える膀胱全摘を回避または遅らせることができる治療として期待されています。
ナドファラゲン フィラデノベクはインターフェロンアルファ2b遺伝子を含む非複製型アデノウイルスベクター。3カ月ごとにカテーテルを使って膀胱内に直接注入する治療で、インターフェロンアルファ2bを高濃度に発現させることで抗がん作用を発揮します。
国内で20人の患者を対象に行われた臨床第3相(P3)試験では、初回投与から3カ月後に完全奏効率75%を達成。23年に「ADSTILADRIN」の製品名で発売された米国では、メイヨークリニックのリアルワールドデータで79%(3カ月)の完全奏効率が示されています。フェリング・ファーマのジョン・プルバー社長は「膀胱全摘除術という選択肢がなかった状況にナドファラゲン フィラデノベクは光明をもたらす。新たな標準治療、中心的治療として確立したい」としています。
関連記事:フェリング・ファーマ、膀胱がん遺伝子治療を26~27年にも日本市場に投入…プルバー社長「向こう3年で年平均15%成長」
一方のTAR-200は、ゲムシタビンを膀胱内に持続的に局所送達するシステム。外来でカテーテルを使って膀胱内に挿入し、挿入後は3週間、留置され、ゲムシタビンを持続的に放出します。申請の根拠とした国際共同P2b試験(コホート2)では、完全奏効率82.4%、奏功期間の中央値25.8カ月を示しました。承認されれば抗がん剤を膀胱内に局所送達する国内初の膀胱内システムとなります。米国では9月9日に「INLEXZO」の製品名で承認されました。
後続には腫瘍溶解性ウイルスや免疫チェックポイント阻害薬
筋層非浸潤性膀胱がんでは、これらに続く新薬の開発も進められています。
キッセイ薬品工業は20年、米CGオンコロジーから腫瘍溶解性ウイルス「CG0070」の中国を除くアジア20カ国の独占的開発・販売権を取得。翌年にはCG社が行う国際共同P3試験に参加し、日本での開発を開始しました。対象はBCG療法が無効の上皮内がんを伴う患者で、主要評価項目は完全奏効率。キッセイは29年度までの現在の中期経営計画期間中の発売を計画しています。
免疫チェックポイント阻害薬の開発も行われており、アストラゼネカの抗PD-L1抗体「イミフィンジ」(一般名・デュルバルマブ)とMSDの抗PD-1抗体「キイトルーダ」(ペムブロリズマブ)がそれぞれ適応拡大に向けたP3試験を実施中。キイトルーダは20年に米国で、BCG不応性で膀胱全摘術が不適格または希望しない高リスク筋層非浸潤性膀胱がんへの適応拡大が承認されています。
ファイザーは新規の抗PD-1抗体「PF-06801591」(ササンリマブ)のP3試験を行っています。
あわせて読みたい
オススメの記事
-

リリー「オルミエント」内用懸濁液が承認/Axcelead DDP、創薬支援強化へ独Proterosと戦略的協業 など|製薬業界きょうのニュースまとめ読み(2026年3月16日)
-

【2025年版】製薬企業なんでもランキング―売上高・研究開発費・年収・従業員数・承認取得数
-

MRの転職市場、スペシャリティ領域中心に活気…開発・製造も採用堅調|製薬業界 今月の転職求人動向レポート(2026年3月)
-

2025年 国内新薬承認取得数ランキング…1位は10承認のヤンセンファーマ、新規有効成分も4成分でトップ
-

内資系CROのパイオニア、イーピーエスが海外事業拡大へ取り組み加速…要となる「グローバルPM」の仕事と魅力とは【AD】








